Вода (альтернативное название: гидроксид водорода) — одно из самых важных для земной жизни веществ. Масса всех водных запасов составляет всего 0,0244% от массы Земли, но вода покрывает около 71% поверхности планеты и составляет основу всех организмов. В этой статье мы разберем строение молекулы воды, а также ее химические и физические свойства.
Роль воды в жизни человека
Вода составляет значительную часть человеческого тела (среднее значение — 55–60% от всей массы). Она выполняет множество жизненно важных функций: обеспечивает обмен веществ, помогает поддерживать стабильную температуру, участвует в синтезе необходимых для жизни веществ, создает гидратную оболочку вокруг ДНК, способствует выведению продуктов обмена.
Распределение воды в тканях неравномерно:
- в крови содержится 75–80% воды, благодаря чему эта соединительная ткань сохраняет текучесть и эффективно снабжает органы необходимыми веществами;
- мозг на 70–75% состоит из воды; ее дефицит способен негативно сказаться на концентрации и памяти;
- стекловидное тело глаза — 98%. Это почти чистая вода;
- в костях около 20–30% — это необходимо для сохранения прочности и эластичности;
- зубы отличаются наименьшим содержанием влаги — в зубной эмали всего 1–2% воды, что придает ей высокую твердость.
Соблюдение водного баланса — залог нормальной работы организма и хорошего самочувствия.
Строение молекулы воды
Молекула воды (H2O) образована одним атомом кислорода и двумя атомами водорода. В процессе образования связей неспаренные электроны атомов (один у каждого атома H и два у атома O) формируют две общие электронные пары по обменному механизму, что приводит к возникновению ковалентных полярных связей.
Наличие двух неподеленных электронных пар на атоме кислорода вызывает отклонение от линейной геометрии: валентный угол ∠HOH составляет 104,5°.
Асимметричное распределение электронной плотности, обусловленное более высокой электроотрицательностью атома кислорода, приводит к формированию частичных зарядов: положительных на атомах водорода и отрицательного на атоме кислорода. Такая асимметрия делает молекулу воды диполем.
Водородная связь
Этот тип связи представляет собой взаимодействие между соседними молекулами воды. Ее возникновение обусловлено наличием в молекуле воды атома кислорода, который сильно притягивает электроны. В результате связь между H и O в молекуле воды становится полярной. На кислороде появляется небольшой отрицательный заряд, а на водороде — положительный. Положительно заряженный атом H одной молекулы «притягивается» к отрицательно заряженному кислороду соседней молекулы.
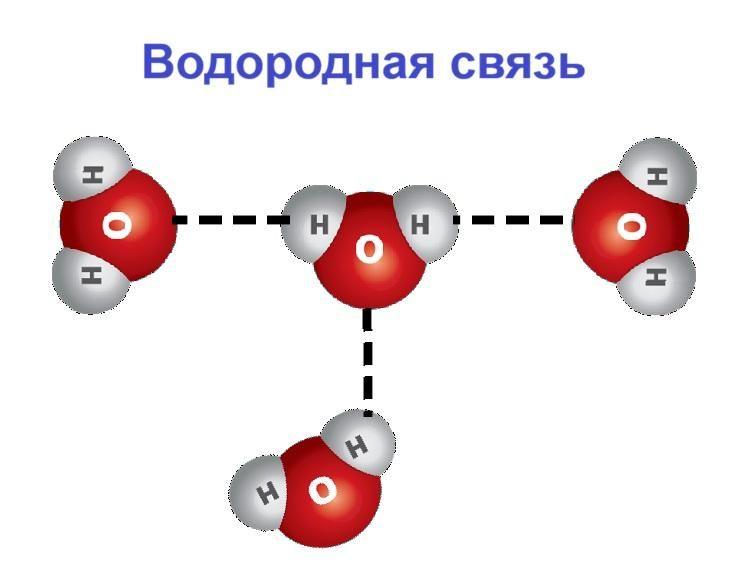
На рисунках такую связь обычно показывают точками или пунктиром.
Физические свойства воды
При комнатной температуре и атмосферном давлении чистая вода представляет собой прозрачную бесцветную жидкость с крайне низкой вязкостью. Не имеет ни вкуса, ни запаха. Закипает при 100°C. Замерзает при 0°C (температура кристаллизации), образуя лед.
При замерзании вода расширяется, а плотность льда оказывается ниже, чем у жидкой фазы, поэтому льдины плавают на поверхности. Благодаря этому свойству воды водоемы зимой не промерзают до дна, сохраняя жизнь обитателям.
Теплоемкость воды при температуре 20°C — 4182 Дж/(кг·°C). Это больше, чем у таких металлов, как медь, латунь, цинк. Поэтому вода медленно нагревается и остывает, регулируя климат: океаны и моря смягчают температурные перепады зимой и летом.
На нашей планете вода существует в трех агрегатных состояниях: твердом (лед), жидком, газообразном (пар). Это обусловлено расстоянием Земли от Солнца — 149,6 млн км. При расстоянии менее 134 млн км вода бы испарилась, а при более 166 млн км — полностью замерзла.
Химические свойства воды

Вода — бинарное неорганическое соединение, в котором кислород находится в степени окисления −2, а водород — в степени +1. Это значит, что воду можно назвать оксидом водорода. Также ей подходит название гидрид кислорода.
Многие соли образуют кристаллогидраты при взаимодействии с водой.
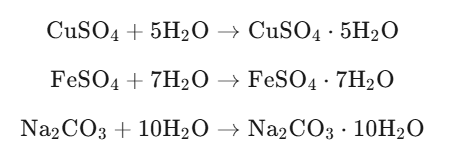
Взаимодействие с металлами (щелочными и щелочноземельными), например, с натрием или кальцием (металл + вода), часто протекает настолько бурно, что может сопровождаться вспышкой.

Взаимодействие с неметаллами (галогенами) протекает по-разному: фтор реагирует бурно, тогда как реакция с йодом практически не идет.

Взаимодействие с оксидами может приводить к образованию кислот или оснований.
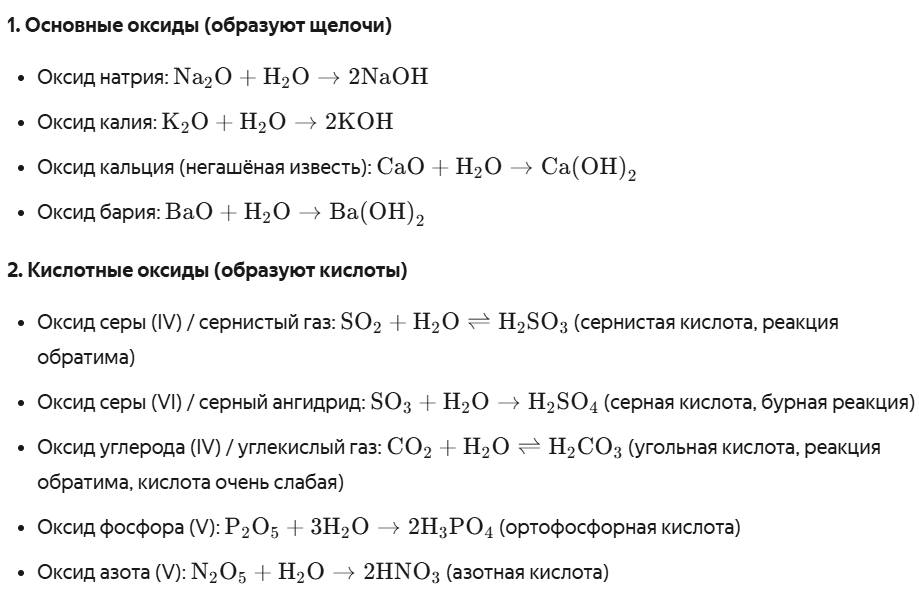
Вода может взаимодействовать со многими металлами, неметаллами, оксидами, солями, карбидами, нитридами, фосфидами и другими веществами. Также она может расщеплять сложные вещества на более простые части. Этот процесс носит название гидролиз. Кроме того, вода — универсальный растворитель, она создает условия для электролиза других веществ.
Заключение
Вода — уникальное вещество с особой молекулярной структурой, определяющей ее свойства. Она обладает высокой теплоемкостью, поверхностным натяжением, способностью растворять многие соединения. Аномалии физических характеристик, а также реакционная способность делают воду абсолютно необходимой для жизнедеятельности любых организмов.


